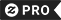Pulsa / haz clic en la imagen para ver más RealViewsMarca registrada
2,15 €
por postal
Postal Elemento individual boron de la tabla periódica
Cant:
Tipo de papel
Mate signatura
18 pt de grosor / 120 lb de peso. Blanco suave, textura suave tipo cáscara de huevo.
-0,20 €
Atribución
Sobre Postcards
Vendido por
Sobre este diseño
Postal Elemento individual boron de la tabla periódica
El cuadro с de los elementos químicos (también el cuadro de Mendeleev, el cuadro periódico de los elementos o el cuadro periódico) es un cuadro tabular de los elementos químicos. Aunque existen precursores de esta tabla, su invención se acredita generalmente al químico ruso Dmitri Mendeleev en 1869, que pretendía ilustrar las tendencias recurrentes ("periódicas") en las propiedades de los elementos. El diseño del cuadro se ha perfeccionado y ampliado con el tiempo, a medida que se han descubierto nuevos elementos, y se han desarrollado nuevos modelos teóricos para explicar el comportamiento químico. La tabla periódica ahora es ubicua dentro de la disciplina académica de la química, proporcionando un marco extremadamente útil para clasificar, sistematizar y comparar todas las muchas formas diferentes de comportamiento químico. La tabla ha encontrado una amplia aplicación en química, física, biología e ingeniería, especialmente en ingeniería química. El cuadro estándar actual contiene 117 elementos en julio de 2009 En 1789, Antoine Lavosier publicó una lista de 33 elementos químicos. Aunque Levisier agrupó los elementos en gases, metales, no metales y tierras, los químicos pasaron el siglo siguiente buscando un esquema de clasificación más preciso. En 1829, Johann Wolfgang Döbereiner observó que muchos de los elementos podían agruparse en tríadas (grupos de tres) basándose en sus propiedades químicas. El litio, el sodio y el potasio, por ejemplo, se agruparon como metales reactivos y blandos. Döbereiner también observó que, cuando se arreglaba por peso atómico, el segundo miembro de cada tríada era aproximadamente el promedio de la primera y la tercera. Esto se conoció como la Ley de las tríadas. El químico alemán Leopold Gmelin trabajó con este sistema, y para 1843 había identificado diez tríadas, tres grupos de cuatro y un grupo de cinco. Jean Baptiste Dumas publicó un trabajo en 1857 describiendo las relaciones entre diversos grupos de metales. Aunque varios químicos pudieron identificar las relaciones entre pequeños grupos de elementos, aún no habían creado un esquema que abarcara a todos ellos. El químico alemán August Kekulé había observado en 1858 que el carbono tiene una tendencia a vincularse con otros elementos en una proporción de uno a cuatro. El metano, por ejemplo, tiene un átomo de carbono y cuatro átomos de hidrógeno. Este concepto finalmente se conoció como valencia. En 1864, el químico alemán Julius Lothar Meyer publicó una tabla de los 49 elementos conocidos arreglados por valencia. La tabla reveló que los elementos con propiedades similares a menudo compartían la misma valencia. El químico inglés John Newlands publicó una serie de artículos en 1864 y 1865 que describían su intento de clasificar los elementos: Cuando se enumeraban en orden de aumentar el peso atómico, se repetían propiedades físicas y químicas similares a intervalos de ocho, que comparaba con las octavas de la música. Sin embargo, esta ley de octavas fue ridiculizada por sus contemporáneos[8]. Retrato de Dmitri Mendeleev, profesor ruso de química, Dmitri Ivanovich Mendeleev y Julius Lothar Meyer, publicaron independientemente sus tablas periódicas en 1869 y 1870, respectivamente. Ambos construyeron sus mesas de manera similar: enumerando los elementos de una fila o columna en orden de peso atómico y comenzando una nueva fila o columna cuando las características de los elementos comenzaron a repetirse. El éxito de la mesa de Mendeleev vino de dos decisiones que tomó: La primera era dejar lagunas en el cuadro cuando parecía que aún no se había descubierto el elemento correspondiente. Mendeleev no fue el primer químico en hacerlo, pero fue un paso más allá al usar las tendencias en su tabla periódica para predecir las propiedades de esos elementos faltantes, como el gallio y el germanio. La segunda decisión consistió en hacer caso omiso ocasionalmente del orden sugerido por los pesos atómicos y cambiar los elementos adyacentes, como el cobalto y el níquel, para clasificarlos mejor en familias químicas. Con el desarrollo de teorías de la estructura atómica, se hizo evidente que Mendeleev había enumerado inadvertidamente los elementos en orden de aumentar el número atómico. Con el desarrollo de teorías mecánicas cuánticas modernas de configuraciones de electrones dentro de los átomos, se hizo evidente que cada fila (o periodo) del cuadro correspondía al llenado de una cáscara cuántica de electrones. En la tabla original de Mendeleev, cada periodo era de la misma longitud. Sin embargo, debido a que los átomos más grandes tienen más subconchas de electrones, las mesas modernas tienen períodos cada vez más largos más abajo en la mesa. En los años que siguieron a la publicación de Mendeleev de su tabla periódica, las brechas que dejó fueron cubiertas a medida que los químicos descubrieron más elementos químicos. El último elemento natural que se descubrió fue Francium (referido por Mendeleev como eka-cesio) en 1939. La tabla periódica también ha crecido con la adición de elementos sintéticos y transuranicos. El primer elemento transurano que se descubrió fue el neptunio, que se formó mediante el bombardeo de uranio con neutrones en un ciclotrón en 1939 "Tabla periódica de elementos" Tabla periódica de elementos Dmitri Mendeleev Antoine Lavosier Químicos Químicos Químicos Química Física Experimentos de laboratorio Poster de gráfico Agosto Kekulé Material Analítico Bioquímica Bioquímica Biología Biológica Biológica Compuestos compuestos Molécula Mole Molecular Avogadro Fórmula Símbolo "Símbolo químico" Átomo Atómico "Peso atómico" Proton Neutron Electron Deuterium Tritio Isómero Molaridad Nucleus Radioactivo Espina Orbital Quantum Período de Fila de Aluminio Americio Antimona Argón ic Astatina Barium Berkelium Beryllium Bismuth Bohrium Boron Bromine Cadmium Calcium Californium Carbon Cerium Cesium Chlorine Chromium Cobalt Curium Darmstadtium Duenio Dysprosium Einsteinium Erbium Fermium Fluorine Francium Gadolinio Gallium Germanium Gold Hafnium Hafnium um Helium Holmium Hidrogeno Indium Yodine Iron Iridium Iron Krypton Lawrencium Lead Lithium Lutetium Magnesium Manganese Meitnerium Mendelevium Mercury Molybdenum Neodimio Neodimio Neptunium Nickel Niobium Nitrogen Nobelium Osmium Oxygen Palladium Foshorus Platinum Plutonio Suero Potasio Praseodimio Prometio Protactinio Radio Radicón Renio Rhodium Rubidium Ruthenium Rutherfordium Samarium Scandium Seaborgium Selenium Silicio Plata Sódico Sestroncio Azufre Tantalio Tellurio Talio Thorium Thulium TinTitanium Tungsten Ununbium nilio Ununumio Uranio Vanadio Xenón Esterbio (itrio) Zinc Zirconio
Traducción automática
Reseñas de clientes
3.6 de 5 estrellas18 Reviews totales
18 opiniones
Reseñas de productos similares
5 de 5 estrellas
Por Anónimo31 de diciembre de 2025 • Compra verificada
Postal, Tamaño: Postal estándar, Papel: Mate signatura, Sobres: Ninguno
El primer envío no llego (tarifa económica) pero tras reclamarlo, me lo reenviaron. El reenvío fue por express sin coste adicional. Ha llegado perfectamente. La calidad de loa productos buena. .
5 de 5 estrellas
Por Pilar A.13 de octubre de 2016 • Compra verificada
Postal, Tamaño: Postal estándar, Papel: Mate signatura, Sobres: Ninguno
Reseña del creador
Para acompañar a mis regalos, me gusta añadir una tarjeta postal con una dedicatoria personal, siempre me lo agradecen!!! Colores muy bonitos, mejor que en la presentación online. me encanta!!!
5 de 5 estrellas
Por Cristina S.8 de abril de 2021 • Compra verificada
Postal, Tamaño: Postal estándar, Papel: Mate signatura, Sobres: Ninguno
Reseña del creador
el prodocto esta muy bien, me gusta mucho, gracias. la impresion me parece muy buena
Etiquetas
Información adicional
Número del producto: 239877814967025216
Creado el: 7/1/2013 9:52
Clasificación: G
Productos vistos recientemente